01
EUDAMED数据库涉及哪些注册?
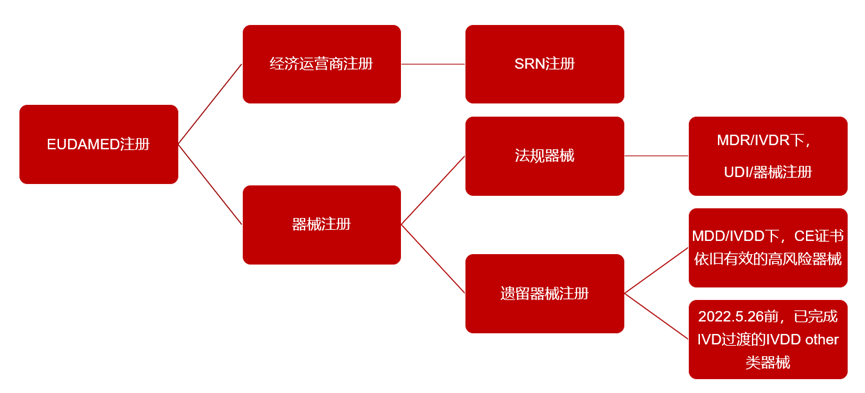
目前EUDAMED数据库可以分成以下3类注册:
1) SRN注册
2) 法规器械注册
3) 遗留器械注册
其中:
SRN的英文全称是Single Registration Number(唯一注册码),是指每个经济运营商在欧盟医疗器械数据库EUDAMED以及相关官方文件和报告上的唯一身份标识;
法规器械注册是指MDR/IVDR法规下的UDI/器械注册,即UDI注册等同于器械注册;
遗留器械注册是指MDD/IVDD下,高风险CE证书依旧有效的风险器械注册,以及在2022年5月26日前已完成IVD过期的IVDD Other类产品的申报。

对于遗留器械,EUDAMED指南中已明确制造商有负责注册的义务。
02
器械注册的流程及所需资料

03
查询方式
已申报器械查询:https://ec.europa.eu/tools/eudamed/#/screen/search-device


04
申请周期
在EUDAMED数据库中,器械申报一旦提交成功,可在查询界面马上查到,无等待时间。